*仅供医学专业人士阅读参考


蔡老师终于带着她的40Hz重回顶刊了,真是好久不见了。前几天编辑们还在讨论,蔡立慧的研究怎么做了3期没有下文了,可别不行了吧。怪不得编辑瞎想,咱们先来简单回顾一下40Hz发迹历程↓
2021年2期临床研究初步数据:阿尔茨海默病治疗重大突破!MIT神经科学大牛的无创黑科技2期临床数据公布,6个月治疗显著延缓认知功能下降83% | 临床大发现
2016年《自然》关键论文:MIT神经学大牛关于阿尔茨海默病的超级颠覆研究,简直简直简直逆天了丨奇点猛科技
2019年《细胞》40Hz声刺激同样有效:《细胞》:膜拜大神!MIT大牛再发阿尔茨海默病颠覆性研究成果,40赫兹的声音可消除AD小鼠大脑β淀粉样蛋白,改善认知丨科学大发现
底层机制论文:《细胞》子刊:再拜大牛!MIT蔡教授团队发现40赫兹LED治疗阿尔茨海默病机制,全球首个临床研究已经开展丨科学大发现
光看标题都能感觉出来,方法是相当简单,效果是相当好,进展是相当快,前景是相当明朗。但备受瞩目的临床试验至今未有数据发布(新冠疫情耽误了可以理解),去年又出现了一篇论文无法完全复现蔡团队的成果,当时的研究者们提出,40Hz多感官刺激可能并非大脑调控的底层机制,面对个体表现差异化极大的阿尔茨海默病(AD),它可能无法普遍起效。
不过今天发布在《自然》杂志上的新成果提供了40Hz刺激疗法的新机制。蔡立慧团队发现,40Hz多感官刺激能够促进AD小鼠脑脊液(CSF)和间质液(ISF)交换,加速淀粉样蛋白的淋巴清除。
令人信心倍增的是,《自然》同期发表了来自华盛顿大学团队的另一篇论文,研究者们同样发现了神经元电位活动能够加速CSF-ISF灌注,一定程度上支持了蔡团队的结论。


论文题图
进入论文之前,我们先来讲讲脑淋巴的故事。大脑中有数以千计的神经元在积极活动,它们通过放电组织人体的运动、思想和行为,这个行为也产生了大量的大脑垃圾。脑淋巴就是清除这些垃圾的重要系统。
脑淋巴允许大脑周围的脑脊液进入动脉旁的血管周围空间,在这里脑脊液与神经元周围的间质液进行物质交换,包括各种离子、神经递质和调节分子、还有代谢垃圾,间质液中的废物可以通过静脉血管周围空间排出。
这个过程中,星形胶质细胞表达的水通道蛋白-4(AQP-4)是很关键的。星形胶质细胞会与血管形成接触面,在这个接触面上AQP-4充当了水的通道。
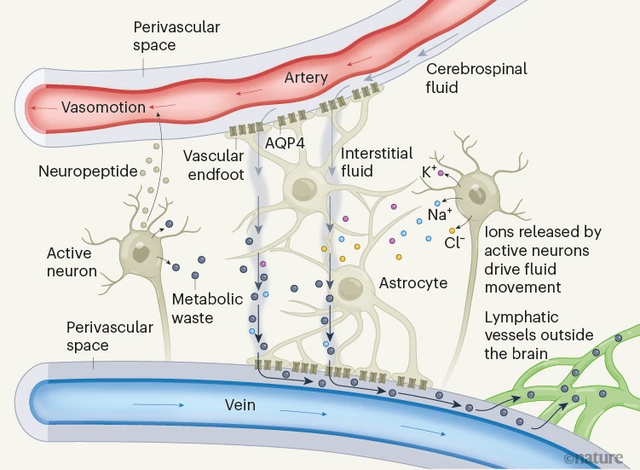
脑淋巴作用机制
曾有研究发现,睡眠和麻醉期间脑脊液流入速率变化,显然不同的大脑节律会影响淋巴转运。如此说来,会影响神经元放电的40Hz刺激,也有可能会改变脑淋巴。
研究者在6个月大的5xFAD小鼠中进行实验,40Hz多感官刺激能够显著减少大脑淀粉样蛋白负荷。监测脑脊液动力学结果发现,40Hz刺激后,小鼠脑脊液流入和间质液外排显著增加。
当研究者使用小分子抑制剂破坏AQP-4功能,脑脊液流入减少、淀粉样蛋白负荷增加。显然,40Hz刺激真的可以促进淀粉样蛋白的淋巴清除。
由于动脉血管运动能够调节脑脊液运动并且会被γ节律影响,研究者在小鼠前额叶皮层处固定了双光子成像,观测小鼠的动脉直径变化。
在40Hz多感官刺激1小时后,小鼠动脉搏动显著增加,血管收缩幅度变大、频率也增快了。动脉的加速搏动显然会加速血管周围空间中脑脊液的流动。
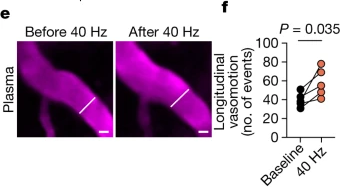
40Hz刺激后血管搏动增加
研究者对刺激后的小鼠脑细胞进行了单核RNA测序,发现星形胶质细胞末端足上与脑脊液运输有关的钾通道Kcnk1表达增加;免疫组化分析也发现,AQP-4极化增加。进一步分析发现,这一过程通过VIP神经元神经肽信号实现。
同期发表的另一篇论文则发现,睡眠和麻醉期间出现的神经元同步放电可以加速脑脊液灌注。虽然这项研究并未提及特定神经元活动频率的影响,但也不能排除不同大脑区域具有一个最佳频率的可能。
无论如何,脑淋巴如何清除大脑垃圾,是会对包括AD在内多种神经退行性疾病产生影响的问题,如何能够有效利用这个清除系统,可以为治疗疾病带来新的思路。
参考资料:
[1]https://www.nature.com/articles/s41586-024-07132-6
[2]https://www.nature.com/articles/s41586-024-07108-6
[3]https://www.nature.com/articles/d41586-024-00422-z


本文作者丨代丝雨
评论列表 (0条)